Поздрав становници наше странице!
Из године у годину производња нафте постаје све сложенија, а гориво добијено из ње све скупље. У земљама ЕУ углавном прете да престану производити бензинске моторе, а сва возила желе заменити електричним аутомобилима. Али литијумске батерије су још увек далеко од идеалних, и успут, уопште се не жури да постану идеалне. У најбољем случају, једним пуњењем литијумске батерије биће могуће превалити удаљеност од максимално 700 км, након чега ћете морати напунити батерију отприлике недељу дана, а ако за пуњење користите обичну утичницу, обично вам треба доста времена. И само замислите шта ће се догодити ако сви почну стално пунити своје електричне аутомобиле, која ће бити огромна оптерећења електроенергетске мреже и колико напона ће се трошити. Генерално, будућност литијумских батерија је још увек прилично неодређена и сваке године се све више истраживања посвећује тражењу нових опција батерија.
Као што знате, најинтензивнији метал је алуминијум. Већ у наше време на неким прототипима алуминијумских батерија можете прећи око 2000 км без поновног пуњења, а поновно пуњење ове врсте батерије траје свега 15 минута, након чега можете прећи још око 2000 км.
Пуњење алуминијумских батерија разликује се од поновног пуњења литијумских батерија. Без обзира на то, у томе нема ништа компликовано, само морате да убаците нови алуминијум, излите електролит и улите нови електролит, све је у основи исто као и бензин аутомобил, само ово је електрични аутомобил и нема оптерећења на електричној мрежи. Поред тога, не морате да производите огроман број утичница са жицама огромног пресека да бисте напунили све ове електричне аутомобиле.
Али овде није све тако глатко. Добијање струје из алуминијума није нимало лако као што бисмо жељели. Прво, разјаснимо шта је принцип алуминијумске батерије.
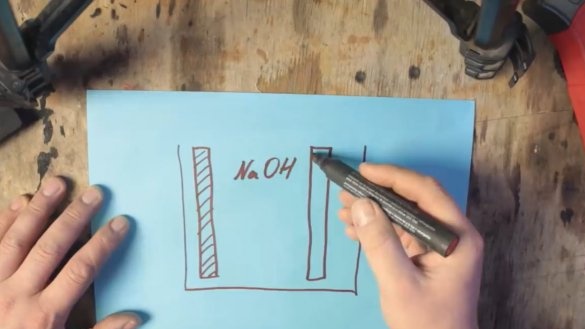
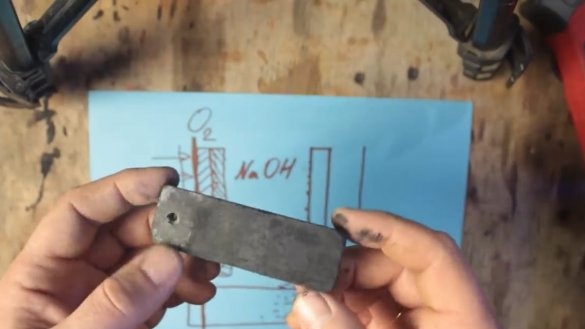
Да би таква батерија почела да ради, биће потребне две електроде: једна природно из алуминијума, а друга из графита. Обе ове електроде су у раствору електролита.
Со (НаЦл) се може користити као електролит, али с њом можете подићи напон на око 0,7 В. Напон алкалног електролита (НаОХ) може се већ повећати на око 1В.
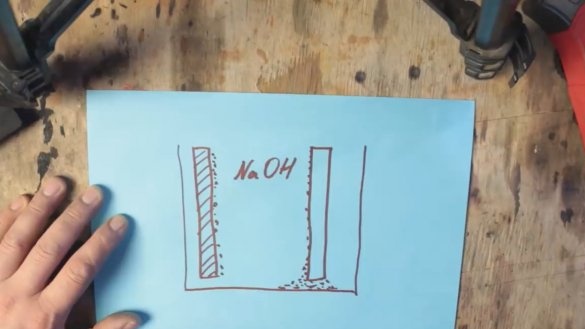
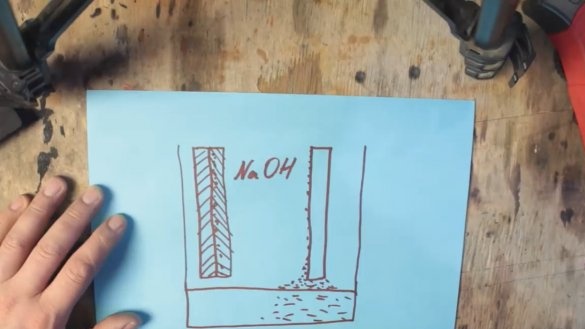
За време хемијске реакције, алуминијум је премазан слојем алуминијум хидроксида (Ал (ОХ) 3), који постепено тоне на дно резервоара. А на површини графитне електроде настају водонични мехурићи, што заузврат доводи до повећања отпора и пада напона, овај процес се назива поларизација.
Први проблем са таложењем алуминијум хидроксида може се отклонити једноставним повећањем капацитета на коме се троши трошени производ, али други проблем може да помогне деполаризациона маса на бази мангановог оксида, која ће се током рада претворити у манган-хидроксид.
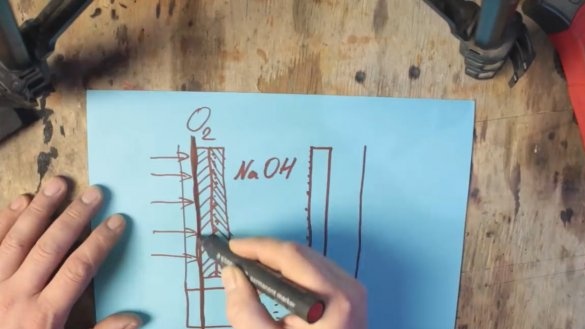
У ствари, добили смо обичну алкалну батерију, али само врло велику. Али појављује се нови проблем. Чињеница је да се троши и манганов оксид, који ће такође морати да се мења. И морамо осигурати да се троши само алуминијум. Да бисте то учинили, узмите кисеоник из околног ваздуха. Ту почињу алуминијумске батерије. Један од зидова само треба заменити плинопропусном мембраном, а графитну електроду треба заменити мешавином графитног и мангановог оксида са наночестицама платине или сребра.
Манганов оксид са наночестицама племенитих метала не реагује, већ делује као катализатор, због чега водоник из електролита оксидира кисеоником у ваздуху.
Технологија за производњу мангановог оксида са укљученим наночестицама сребра у принципу није компликована и може се испробати у занатским условима. Али у овом чланку ћемо расправљати о томе како да направите најисплативију опцију за батерију која прима енергију од алуминијума. Следећа упутства су преузета са сајта Фиери ТВ ИоуТубе. Више детаља у оригиналном ауторском видеу:
Верзија графита са максималним буџетом су летњи контактни умеци за тролејбусе. На крајњим тролејбуским стајалиштима могу се пронаћи апсолутно бесплатни, или их можете купити, нису скупе, аутор их је пронашао у продаји по цени од 22 рубље по комаду.
Даље, потребна нам је алкалија. Ево алата за чишћење цеви у свом саставу садржи сто процентних натријум алкалија.
За покретање алкалне реакције потребно нам је само мало, 1 г алкалије на 0,5 л воде биће довољно.
Пре свега, хајде да проверимо да ли је графитна електрода заиста потребна у овој батерији. За искуство узмимо ову електроду од нехрђајућег челика.
Сада ставимо алуминијску плочу и електроду од нехрђајућег челика у алкалу, повежемо мултиметар и видимо колико волти испада.
Као што видите, испоставило се да је око 1.4В. Сада проверимо струју кратког споја.
Струја кратког споја показала се у подручју од 20мА. Који закључци се могу извући: теоретски у екстремним условима је могуће саставити батерију шоља од нехрђајућег челика и алуминијумске фолије.
Даље ћемо имати бакарну електроду направљену од електричног бакра.
Као што можемо приметити, напон се показао незнатно вишим од 1,4 В, али је струја кратког споја у почетку била велика, али је затим почела брзо да пропада и бакар је почео да се прекрива тамним премазом, највероватније је овај ефекат изазвао нечистоће у води, пошто вода У овом експерименту, аутор је узео славину из славине.
Сада уроните графитну електроду у раствор електролита.
Помоћу ове електроде добијен је напон од 1,3 В, струја кратког споја зауставила се у подручју од 17 мА. На први поглед чини се да је електрода од нехрђајућег челика ефикаснија, али површина нехрђајуће електроде је већа па није познато који је графит или нехрђајући челик бољи.
Будући да графит има прилично велики отпор, морате се некако носити с њим. Потребно је направити електроде од материјала који добро води, а графит треба да буде само на њеној површини.Одлучено је да се изврши бушење кроз графит и у резултирајућим рупама сечи навој за м6 вијке.
Резултат је челична електрода са графитном шкољком.
Отпор непробушеног графита је око 4,5 Охма, али бушеног графита око 1,7 Охма.
На лицу ће се смањити отпорност, а самим тим и ефикасност структуре. У даљим експериментима користићемо дестиловану воду.
Први експеримент са електролитом, у коме је 4 г алкалије на 1 литар воде.
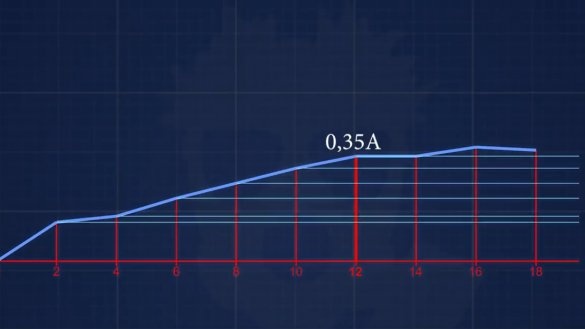
Струја кратког споја је испала 150мА. Следећи електролит има концентрацију 6 г алкалија на 1 литар. Па и тако даље, сваки пут ћемо повећавати концентрацију за 2 г док не постигнемо концентрацију код које се струја неће повећавати.
Иако таква једноставна батерија нема велику ефикасност струје, али таква батерија може радити веома дуго, а било који алуминијум се може користити као електроде, које се лако могу растопити у електроде било ког облика, на пример, алуминијумске лименке разна алкохолна и безалкохолна пића, чоколадна фолија итд.
Као резултат, након свих експеримената са различитим концентрацијама електролита, постаје јасно да овим дизајном батерије нема смисла додавати више од 12 г алкалије у 1 литар воде, односно, добијамо око 1% раствора.
Затим је аутор саставио још један клип, који се састојао од 3 електроде.
Две батерије дају већи напон и мање губитка, тако да је резултат бољи.
Сада узмимо канту електролита, велики комад алуминијума и две електроде од нехрђајућег челика.
У канти концентрација електролита од 10 г / 1л. Највиша струја 1.3А, смањила се на 520мА. Са свом огромном површином од нехрђајућег челика, није се упоредио са графитом, јер се испоставило да је 600мА са графитом. Узгред, током реакције се ослобађа водоник, који се такође може сакупљати и користити као извор енергије. Укратко, има простора за раст. То је за сада све. Хвала на пажњи. Видимо се ускоро!