
Једноставни технички експерименти врло су корисни за децу: ово је заједничко проводење времена, усвајање вештина и разумевање малих дизајнера, основа да хлебци, као у чувеном цртаном филму, не расту на дрвећу.
Овај пут смо одлучили да направимо најједноставнији хемијски извор струје и покушали да га применимо за било шта практично. Када говоримо о практичној примени, вреди подсетити да су пре само неколико генерација радиоаматерима, за снабдевање батеријским пријемницима и појачивачима, били понуђени производи неколико врста галванских ћелија или батерија за самосталну производњу. То су елементи Леклансхеа и Попова [1], стр. 9 ... 18, или оловно-калијева или гасна батерија [1], стр. 22 ... 28. Неколико релативно струјних елемената било је повезано на жаруљу са жарном нити (жаруља са жарном нити), десетине мањих елемената, на анодну батерију, чији напон је могао достићи 60-80 волти. Батерије су биле „мокре“ - са течним електролитом и захтевала негу и одржавање.
Дакле галванска ћелија, неколико речи "како?" и "зашто?" Електрична струја настаје када метали међусобно делују. У овом случају долази до другачије разлике потенцијала (напона). Још 1793. године, Алессандро Волта, конструирајући галванску ћелију (Волта пол), установио је релативну активност тада познатих метала: Зн, Пб, Сн, Фе, Цу, Аг, Ау. Показало се да је "снага" галванске ћелије већа, што даље метали у овом низу су стајали (низ напона).

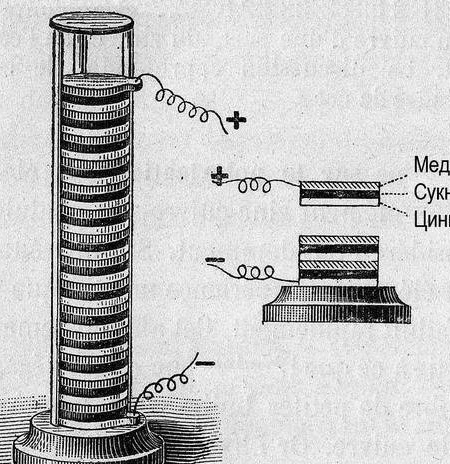
Касније, за организовање података, потенцијал „водоничне електроде“ узет је као нулта референца. После мерења потенцијала метала упарених са њим, експериментални метали су распоређени у низу. Добијена табела названа је "Електрохемијска серија металних напрезања", а у кабинету за хемију мора да виси поред периодичног система и портрета Дмитрија Ивановича.

Бројни напони метала корисна су контрацепција, у нашем случају ћемо, као и Алессандро Волта, знати - што се метали даље одвајају један од другог, већа ће бити напетост.
У нашим експериментима, попут класика, користили смо бакар и цинк.Када су плоче уроњене у електролит, између ње и цинкове плоче, долази до хемијске реакције, услед које се на плочи накупљају негативни набоји и негативно се наелектришу. Као резултат реакције која се одвија у галванској ћелији, цинкова електрода се постепено раствара.
На бакарној електроди током рада галванске ћелије формирају се ситни водонични мехурићи који изолишу површину бакра од електролита. Феномен се назива, у галванској ћелији је штетан, они се с њим боре. Да би се уклонио ослобођени водоник, у електролит се уводе супстанце зване водоник. У њиховој улози често су једињења мангана, бакар сулфата. У једноставним експериментима може се користити апотекарски калијев перманганат.
Шта смо користили за експеримент.
Уређаји и материјали.
За склапање галванских ћелија као бакарних електрода можете користити жицу, жицу, фолију. Цинк се може екстраховати из сувих елемената, могу се користити поцинчани производи. Уместо цинка, можете покушати да користите електроду од алуминијума или гвожђа. Натријум-хлорид за електролит, мало меке монтажне жице. Свакако вам требају волтметар или мултиметар, жичане секаче, маказе. Као посуде могу се користити неметални спремници одговарајуће величине. Стакло, погодније од лаганих пластичних шољица - теже су, стабилније и теже их је оборити. Врло је добро ако постоји оптерећење ниског напона ниског напона - једноставан радио, кварцни сат итд.
Акумулатор од жице и високих напона високог напона.
Фасцинирани једноставношћу детаља и релативно високим примљеним напоном покушали смо саставити такву батерију. Овде се користи „класични“ пар метала - бакар-цинк. Идеја је да се галванизирани затварачи користе као цинкова електрода. Изврсно. Јасно је да такав елемент није предвиђен за дуготрајан рад - танки слој цинка ће се брзо растопити, међутим, то није важно за краткотрајни експеримент. Али поцинчани шрафови или шрафови су свуда пуни.
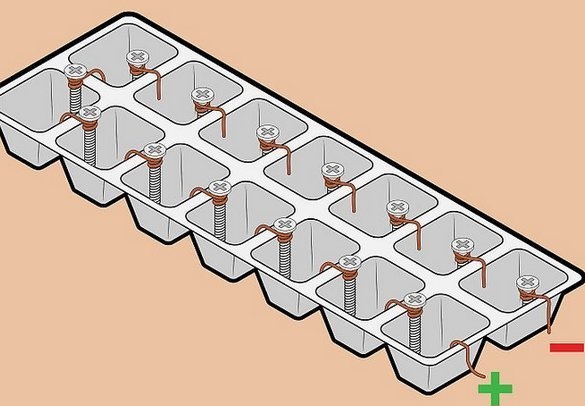
Жица се такође користи као бакарна електрода - такође широко доступан материјал, поред тога - најповољнија инсталација елемената у батерији - сви елементи су повезани серијски - плус један до минус следећег. У овом се случају напон збраја, струја остаје иста.
Почнимо.
Након одабира потребног броја поцинкованих затварача жељене дужине, пронашли смо одговарајућу бакарну жицу. Ово је жица за наматање у изолацији лака. Пречник жице је око 0,5 мм.

Стуб неколико пута очисти изолацију лака, напрежући жицу кроз двоструко пресавијену брусну кожу средње величине.


Затим припрема пар електрода - испод главе саморезног вијка, чврсто омота два или три навоја жице и одреже вишак.

Склоп батерије - корито је коришћено као контејнер за замрзавање леда. Можете користити ћелије из кутијастих слаткиша, међутим, оне су суптилније. Након постављања електрода на зидове између ћелија, спремнике напунимо електролитом. Користили смо раствор кухињске соли - кашику са слајдом од 0,5 литара топле воде. За пуњење је веома погодно користити медицинску штрцаљку.


Пронашли смо још неколико шрафова за електроде и додали елементе батерији, то је оно што имамо. Напон код оптерећења велике импеданце (улазни отпор дигиталног волтметра) је значајан, али при сваком оптерећењу, колико год приметно, значајно пада.
Покушај слична галванска ћелија (батерија) са већим електродама.
Као контејнер користили смо теглу од две литре (две), у коју ће се уградити тањири значајне површине. Као електроде узели смо танку бакарну фолију и цинк - остатке чаше из фабричког "сувог" елемента, растављене током производње графита за ватростални премаз.

Остатке осушених кристалних соли очистили смо жичаном четком и резали две плоче са приближно маказицама са приближно истом површином. Од бакрене фолије изрежите две одговарајуће траке. Такође са шкарама. Добили смо два пара електрода које су наше елементе, без додатног обожавања, савијале њихове ивице на врату лименке.


У већој посуди смо припремили електролит - натријум хлорид, растворен у топлој води, концентрација је иста и припремљени елементи се сипају.


Два елемента спојили смо у серији, користећи део причврсне жице и две копче за крокодиле. Дакле, у реду, напон батерије је близу стандардног „прста“, покушајте да користите. Један елемент са напоном од 1,5 В користи се у електромеханичком сату, осим тога, тренутна потрошња сата је врло мала и наша батерија ће моћи да га надвлада.

Уклонили смо стандардну батерију са сата и спојили на терминале део делова за монтажу. Посматрајући поларитет (бакарна плоча - "+", цинк - "-"), повезали смо сат са импровизованом батеријом, воила! Сат ради, напон "тоне" на 1,3 В. Сат је савршено функционирао неколико сати, све док се сви нисмо похвалили (ма који је чаробњак!), А онда смо се уморили.

На стазу.
Унутрашња конституција било ког детета је таква да пажња на једну тему може да се фокусира не више од 15 ... 20 минута, а све часове са децом треба испланирати тако да се у то време уклапају или прелазе између различитих часова, иначе ћете се обоје мучити.
Као оптерећење је боље применити да ли је покретни или светлосни - бројеви на волтметру импресионирају ум, али не и срце. Осим сатова и калкулатора, засигурно ће изазвати дивљење, рад из кућне батерије малог радио пријемника (као опција - кућни рад!).
За дуготрајну употребу, електролит ћелија треба заштитити од прашине и испаравања и водити рачуна о деполаризатору - добро, бар зачепите теглу комадом пластичне фолије са еластичном траком и додате калијум перманганат у електролит. Штавише, боље је одмах прикупити споменути елемент Попова.
Поред поцинчаних шрафова за саморезне шаре, могуће је користити и поцинковани челични лим, за велике елементе је згодније - за време експеримента можете да добијете значајну струју и снагу шта год (померајући прсте у ваздуху).
Листа коришћене литературе.
1. П. Стрелков. Знати и бити у стању. Пионирски инжењер електротехнике. Детгиз. 1960 год
2. Полосин В., В. Прокопенко. Радионица о методологији наставе хемије. Москва, "Просветитељство", 1989., стр. 202.203.

